Maschinenlesbare Briefings
KI übersetzt unstrukturierte Anforderungen in eine technische, maschinenlesbare Projektanfrage.
Wir verwenden Cookies, um Ihre Erfahrung zu verbessern und den Website-Traffic zu analysieren. Sie können alle Cookies akzeptieren oder nur die notwendigen.
Hör auf, statische Listen zu durchsuchen. Sag Bilarna, was du wirklich brauchst. Unsere KI übersetzt deine Anforderungen in eine strukturierte, maschinenlesbare Anfrage und leitet sie sofort an verifizierte Arzneimittelentwicklung und Compliance-Expert:innen weiter – für präzise Angebote.
KI übersetzt unstrukturierte Anforderungen in eine technische, maschinenlesbare Projektanfrage.
Vergleiche Anbieter anhand verifizierter KI-Vertrauensscores und strukturierter Fähigkeitsdaten.
Überspringe kalte Akquise. Angebote anfordern, Demos buchen und direkt im Chat verhandeln.
Filtere Ergebnisse nach konkreten Rahmenbedingungen, Budgetgrenzen und Integrationsanforderungen.
Minimiere Risiken mit unserem 57-Punkte-KI-Sicherheitscheck für jeden Anbieter.
Verifizierte Unternehmen, mit denen du direkt sprechen kannst
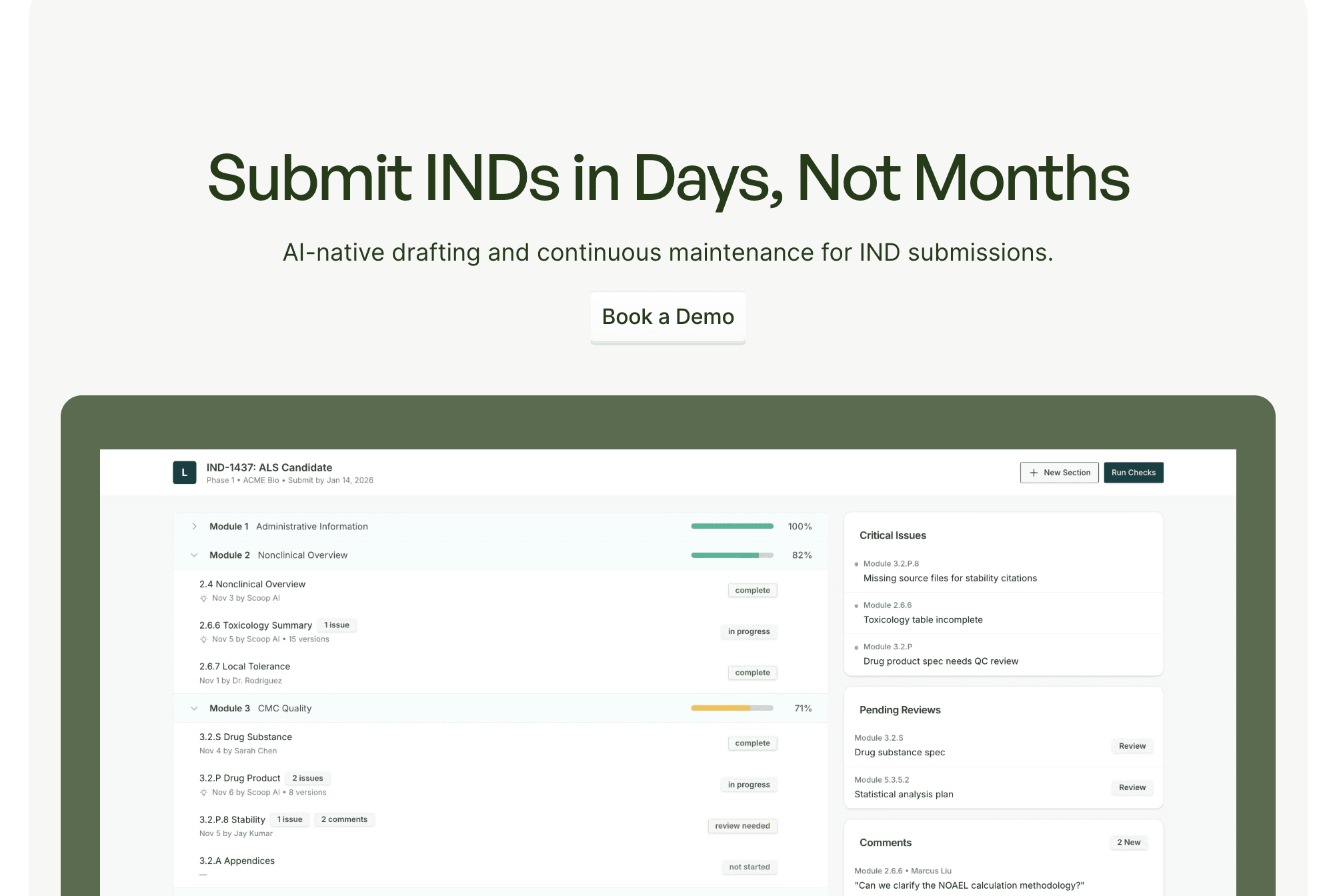
AI platform that speed up drug trials with fast, accurate regulatory filings.
Führen Sie einen kostenlosen AEO- und Signal-Audit für Ihre Domain durch.
Answer-Engine-Optimierung (AEO)
Einmal listen. Nachfrage aus Live-KI-Konversationen konvertieren – ohne aufwendige Integration.
Arzneimittelentwicklung und regulatorische Compliance ist ein strukturierter Rahmen, der die Entdeckung, Prüfung und Zulassung neuer Therapien gemäß gesetzlicher Vorgaben sicherstellt. Der Prozess umfasst präklinische Studien, klinische Phasen und die fortlaufende Überwachung nach dem Markteintritt. Dies gewährleistet Patientensicherheit, Wirksamkeit der Medikamente und legale Marktfähigkeit für Pharmaunternehmen.
Forscher identifizieren einen Wirkstoffkandidaten und testen ihn umfassend im Labor und in Tiermodellen, um erste Sicherheits- und Wirksamkeitsdaten zu sammeln.
Der Kandidat durchläuft drei Phasen klinischer Studien an menschlichen Probanden, um Dosierung, Sicherheit und therapeutische Wirkung zu belegen.
Ein umfassender Zulassungsantrag wird bei Behörden eingereicht, gefolgt von einer fortlaufenden Pharmakovigilanz zur Sicherheitsüberwachung des zugelassenen Produkts.
Start-ups nutzen diese Dienstleistungen, um ihren ersten Wirkstoffkandidaten von der Forschung durch alle regulatorischen Hürden bis zur erfolgreichen Marktzulassung zu navigieren.
Hersteller benötigen Expertise für Abbreviated New Drug Applications (ANDAs), um nach Patentschutzablauf rechtssichere und bioäquivalente Generika auf den Markt zu bringen.
CROs integrieren Compliance in ihr Studiendesign und -management, um Daten zu erheben, die globalen Standards der Zulassungsbehörden vollständig entsprechen.
Unternehmen kombinieren regulatorische Strategien für Arzneimittel und Geräte, um komplexe Kombinationsprodukte wie drug-eluting stents oder autoinjectors zuzulassen.
Etablierte Pharmaunternehmen beauftragen Experten, um ihre bereits zugelassenen Produkte in neuen Regionen gemäß lokaler Vorschriften wie der EMA oder PMDA zu registrieren.
Bilarna bewertet Anbieter für Arzneimittelentwicklung und Compliance mit einem proprietären 57-Punkte-AI-Trust-Score. Dieser analysiert technische Expertise, regulatorische Erfolgsbilanz, Referenzen aus der Branche und die Qualität der Dokumentationsprozesse. Nur Anbieter, die strenge Kriterien in Bereichen wie GxP-Konformität und Audit-Historie erfüllen, werden auf der Plattform gelistet.
Vom Wirkstoffdesign bis zur Marktzulassung dauert es durchschnittlich 10 bis 15 Jahre. Dieser lange Zeitraum umfasst Jahre der Forschung, mehrere Phasen klinischer Studien und die intensive regulatorische Prüfung der Antragsunterlagen durch Behörden.
Die Gesamtkosten belaufen sich schätzungsweise auf 1 bis 2 Milliarden Dollar pro zugelassenem Wirkstoff. Ein großer Teil entfällt auf die kostenintensiven klinischen Studien der Phase III und die umfangreichen Herstellungstests für die regulatorische Dossiererstellung.
Die FDA (USA) und die EMA (EU) haben unterschiedliche rechtliche Anforderungen und Verfahrenswege. Eine FDA-Zulassung ist für den US-Markt erforderlich, während eine EMA-Zulassung den Zugang zum europäischen Markt ermöglicht. Viele Anbieter unterstützen bei der parallelen Einreichung bei beiden Behörden.
Ein vollständiger Antrag, wie ein New Drug Application (NDA), umfasst Zehntausende Seiten. Kernbestandteile sind die klinischen Studienergebnisse (CTD Module 5), Qualitätsdaten zur Herstellung (Module 3) und umfassende nicht-klinische Sicherheitsberichte (Module 4).
Priorisieren Sie Anbieter mit nachgewiesener Erfahrung in Ihrer spezifischen Therapeutika-Klasse und Zielregion. Entscheidende Kriterien sind ein starkes Team aus ehemaligen Behördenmitarbeitern, eine transparente Erfolgsbilanz bei Einreichungen und robuste Qualitätsmanagementsysteme (QMS).
Nein, eine Registrierung ist nicht erforderlich, um ein kostenloses KI-gestütztes Website-Compliance-Audit-Tool zu verwenden. So nutzen Sie es sofort: 1. Besuchen Sie die Website des Audit-Tools. 2. Geben Sie die URL Ihrer Website in das vorgesehene Feld ein. 3. Starten Sie den Compliance-Scan sofort ohne Kontoerstellung. 4. Warten Sie einen Moment, bis die KI Ihre Seite analysiert. 5. Erhalten Sie sofortige Ergebnisse und einen detaillierten Compliance-Bericht ohne Anmeldevorgang.
KI-Compliance-Plattformen sind darauf ausgelegt, Zollmakler im Importprozess zu ergänzen, nicht zu ersetzen. Diese Plattformen bieten automatisierte Prüfungen und Klassifizierungsempfehlungen, um Fehler und potenzielle Einsparungen zu identifizieren, aber sie reichen keine Zollanmeldungen, Korrekturen oder Unterlagen bei den Zollbehörden ein. Lizenzierte Zollmakler bleiben für die Einreichung von Anmeldungen und die Abwicklung offizieller Kommunikation unerlässlich. Die KI-Plattform liefert belastbare Nachweise und Erkenntnisse, die Makler nutzen können, um Genauigkeit und Compliance zu verbessern, wodurch der gesamte Importprozess verbessert wird, ohne die Rolle des Maklers zu ersetzen.
CMMC (Cybersecurity Maturity Model Certification) Compliance ist für Unternehmen in der Verteidigungs-Lieferkette entscheidend, da sie eine verbindliche Voraussetzung ist, um Angebote für Verträge des US-Verteidigungsministeriums (DoD) abgeben und diese erhalten zu können. Sie bestätigt, dass ein Unternehmen die notwendigen Cybersicherheitspraktiken zum Schutz von Federal Contract Information (FCI) und Controlled Unclassified Information (CUI) implementiert hat. Das Erreichen der Konformität, insbesondere Level 2, demonstriert eine robuste Sicherheitslage, die sensible Verteidigungsdaten vor fortgeschrittenen Bedrohungen schützt. Nichteinhaltung kann zum Verlust laufender Verträge und zur Disqualifikation von zukünftigen DoD-Möglichkeiten führen, was sie zu einem grundlegenden Geschäftsimperativ für Verteidigungsauftragnehmer und Subunternehmer macht.
Compliance ist für die Entwicklung digitaler Gesundheitssoftware entscheidend, da sie die Patientensicherheit, Datensicherheit und den rechtmäßigen Betrieb in stark regulierten Gesundheitsmärkten gewährleistet. Software, die persönliche Gesundheitsinformationen (PHI) verarbeitet, muss strenge Datenschutzvorschriften wie die DSGVO in Europa oder HIPAA in den USA einhalten. Wenn die Software zudem als Medizinprodukt fungiert oder mit einem solchen integriert ist, muss sie spezifische Softwareentwicklungslebenszyklen (SDLC) und Standards für Medizinprodukte befolgen. Nichteinhaltung kann zu schweren rechtlichen Sanktionen, Vertrauensverlust bei Nutzern und Marktausschluss führen. Daher integrieren Entwicklungsprozesse von Anfang an Compliance-Beratung, die sich mit Datensicherheitsstandards, sicheren Datenintegrationspraktiken und der Beschaffung notwendiger Zertifizierungen befasst, um vertrauenswürdige und rechtlich tragfähige Lösungen für Patienten, Anbieter und Versicherer zu schaffen.
Compliance ist im Marketing für medizinische Ästhetik von entscheidender Bedeutung, da sie sicherstellt, dass alle Werbematerialien und -aussagen strengen Werberichtlinien im Gesundheitswesen und ethischen Standards entsprechen, wodurch die Klinik vor rechtlichen Strafen und Imageschäden geschützt wird. Das Marketing in diesem Sektor muss unbewiesene Aussagen über Behandlungsergebnisse vermeiden, die von Behörden wie der FDA in den USA oder der MHRA in Großbritannien als irreführend angesehen werden könnten. Eine konforme Strategie konzentriert sich auf Bildungsinhalte, transparente Preisgestaltung und genaue Darstellungen der Qualifikationen der Behandler. Sie umfasst auch ordnungsgemäße Einwilligungsverfahren der Patienten und Datenschutz gemäß Vorschriften wie der DSGVO. Die Priorisierung von Compliance mindert nicht nur Risiken, sondern baut auch das Patientenvertrauen auf, indem sie Professionalität und ein Bekenntnis zur Sicherheit demonstriert, was in einem wettbewerbsintensiven Markt ein starkes Differenzierungsmerkmal ist.
Compliance ist in Plattformen zur Verbraucher-Kreditverwaltung entscheidend, um sicherzustellen, dass alle Kreditverwaltungsaktivitäten den gesetzlichen und regulatorischen Anforderungen entsprechen. Dies schützt sowohl den Kreditgeber als auch den Kreditnehmer, indem Risiken im Zusammenhang mit Ausfällen, Datenschutz und fairer Behandlung minimiert werden. Integrierte Compliance-Funktionen helfen bei der Automatisierung von Überwachung und Berichterstattung, wodurch Verstöße und Strafen reduziert werden. Die Einhaltung von Vorschriften stärkt zudem das Vertrauen der Verbraucher und unterstützt nachhaltige Kreditverwaltungsprozesse.
Die Compliance-Aufzeichnung für Microsoft Teams ist von entscheidender Bedeutung, um sicherzustellen, dass alle Kommunikationen den gesetzlichen, behördlichen und internen Corporate-Governance-Standards entsprechen. In Branchen wie Finanzen, Gesundheitswesen und Behörden schreiben Vorschriften häufig die Erfassung, sichere Speicherung und Abrufbarkeit elektronischer Kommunikation für Audits, Streitbeilegung und Rechtsermittlungen vor. Eine spezielle Compliance-Aufzeichnungslösung integriert sich in Microsoft Teams, um Sprach-, Video- und Chat-Interaktionen automatisch zu erfassen. Dieser Prozess schützt die Organisation vor Compliance-Verstößen, die zu erheblichen Geldstrafen und Reputationsschäden führen können. Die Lösung archiviert Aufzeichnungen sicher in einem unveränderlichen Format, oft mit Verschlüsselung und Zugriffskontrollen, und bietet Werkzeuge für effiziente Überwachung, Suche und Abruf. Sie stellt eine überprüfbare Prüfspur sicher, unterstützt Qualitätssicherung und Mitarbeiterschulung und hilft, die Datensouveränität zu wahren, indem sie kontrolliert, wo Aufzeichnungen gespeichert werden.
Cybersicherheits-Compliance ist für Unternehmen von entscheidender Bedeutung, da sie einen strukturierten Rahmen zum Schutz sensibler Daten, zur Minderung rechtlicher und finanzieller Risiken und zum Aufbau von Vertrauen bei Kunden und Partnern bietet. Die Einhaltung von Vorschriften wie der DSGVO, HIPAA, PCI DSS oder branchenspezifischen Standards stellt sicher, dass ein Unternehmen obligatorische Sicherheitskontrollen zur Verhinderung von Datenlecks und Cyberangriffen implementiert. Nichteinhaltung kann zu schwerwiegenden Sanktionen führen, darunter Millionenstrafen, rechtliche Haftung und Reputationsschäden, die ein Unternehmen ruinieren können. Darüber hinaus demonstriert eine robuste Compliance-Haltung die gebotene Sorgfalt gegenüber Stakeholdern, kann sich in Ausschreibungen und Partnerschaften als wettbewerbsentscheidend erweisen und entspricht oft grundlegenden Cybersicherheits-Best Practices, wodurch die gesamte Sicherheitslage einer Organisation über reine Kontrolllisten-Audits hinaus gestärkt wird.
Das Anvisieren von Kinasen wie p38, MK2 und ERK ist schwierig, da diese Enzyme an mehreren zellulären Funktionen beteiligt sind. Eine Spezifität zu erreichen, ohne normale zelluläre Aktivitäten zu stören, ist komplex. Medikamente müssen selektiv die dysregulierten Kinasewege hemmen, die für die Krankheit verantwortlich sind, während sie essentielle zelluläre Prozesse erhalten. Dieses Gleichgewicht zu erreichen ist schwierig und macht die Entwicklung effektiver und sicherer kinasegerichteter Therapien zu einer bedeutenden wissenschaftlichen Herausforderung.
Die Rückverfolgbarkeit von Holz ist für Nachhaltigkeit und gesetzliche Compliance wichtig, da sie sicherstellt, dass Holzprodukte aus verantwortungsvoll bewirtschafteten Wäldern stammen und regulatorische Standards erfüllen. 1. Rückverfolgbarkeit hilft, die Herkunft des Holzes zu verifizieren und verhindert illegale Abholzung und Entwaldung. 2. Sie unterstützt Zertifizierungssysteme wie FSC oder PEFC durch transparente Lieferkettendaten. 3. Ermöglicht Unternehmen die Einhaltung von Gesetzen wie der EU-Holzverordnung oder dem Lacey Act nachzuweisen. 4. Fördert nachhaltige Forstwirtschaft durch Verantwortlichkeit in jeder Phase. 5. Stärkt das Verbrauchervertrauen durch Nachweis ethischer Beschaffung und Umweltverantwortung.